Alcoholes
I.
ALCOHOLES
Los alcoholes se caracterizan por la presencia del grupo funcional
hidroxilo (OH), unido a un átomo de carbono, que a su vez hace parte de una
cadena hidrocarbonada alifática y saturada. Esto implica que los carbonos de
la cadena presentan hibridación sp3. Pueden considerarse como derivados
orgánicos del agua, a través de la sustitución de un hidrógeno un grupo alquilo
(R—OH).
Aquí sólo abordaremos los alcoholes acíclicos saturados, de fórmula general tipo: R-OH, donde R puede ser un grupo alquilo (cadena hidrocarbonada alifática).
Aquí sólo abordaremos los alcoholes acíclicos saturados, de fórmula general tipo: R-OH, donde R puede ser un grupo alquilo (cadena hidrocarbonada alifática).
Antes de profundizar en el estudio de los alcoholes, vale la pena
preguntarse, ¿por qué es importante conocer la química de los alcoholes? De
todos los compuestos orgánicos, tal vez los alcoholes son los más conocidos.
Así, desde la antigüedad se admitía que las propiedades particulares de las
bebidas alcohólicas se relacionaban con la presencia de alcohol etílico o
vínico.
Los alcoholes tienen gran importancia en biología, puesto que la
función alcohol aparece en muchos compuestos relacionados con los sistemas
biológicos. Así, por ejemplo, la mayoría de los azúcares, el colesterol, las
hormonas y otros esteroides contienen alcohol.
Los alcoholes también tienen muchas aplicaciones industriales y
farmacéuticas, como veremos más adelante. A manera de ejemplos, podemos
mencionar algunos de los usos de los alcoholes, como aditivos de combustibles,
solventes industriales y componentes principales de bebidas alcohólicas,
anticongelantes para automóviles y fabricación de barnices.
Pero, de la misma manera que resulta importante conocer el
comportamiento químico de los alcoholes en razón de los múltiples usos y
aplicaciones, también es importante estudiarlos por los efectos nocivos que
pueden producir sobre los organismos y la sociedad. El etanol, por ejemplo,
puede ser considerado como una droga con efectos depresores del sistema
nervioso central. Su ingestión a través de bebidas alcohólicas, provoca una
serie de efectos, como sedación, vasodilatación cutánea, taquicardia,
disminución en el control de las emociones, pérdida de la coordinación motora
y, si la concentración de etanol en la sangre es muy alta, puede producir la
muerte por paro cardiorrespiratorio.
1.1.NOMENCLATURA
IUPAC DE LOS ALCOHOLES.
En el sistema IUPAC, los alcoholes se nombran como alcanoles, es decir, se cambia la terminación (o) del alcano por el sufijo (ol), y sus nombres se forman a partir de una raíz, un sufijo primario (ej: met, et, prop, but, penta, hexa) y un sufijo secundario, por ejemplo:
En el sistema IUPAC, los alcoholes se nombran como alcanoles, es decir, se cambia la terminación (o) del alcano por el sufijo (ol), y sus nombres se forman a partir de una raíz, un sufijo primario (ej: met, et, prop, but, penta, hexa) y un sufijo secundario, por ejemplo:
1. Para nombrar a los alcoholes se elige la cadena más
larga que contenga el grupo hidroxilo (OH).
3. Se nombran los grupos sustituyentes o ramificaciones en orden alfabético
indicando su posición con un número, que corresponda al átomo de carbono
enumerado previamente. En este caso hay un grupo metil en el carbono 4.
En el caso de existan dos o mas sustituyentes se emplean los prefijos numéricos Di, tri, tetra, etc; para indicar que se repite dos, tres y cuatro veces respectivamente.
4.
El nombre de la
cadena principal se obtiene cambiando la terminación –o del alcano
correspondiente por el sufijo –ol. Indicando
además la posición del –OH. Ejemplo:


En este caso, el compuesto recibe el nombre: 4-metil-2-hexanol
Otros ejemplos:
1.2. Formulación de alcoholes.
Para escribir la formula semidesarrollada de un alcohol se pueden realizar los mismos pasos o estrategias que se usan para formular alcanos. (Tema que ya fue abordado en clases presenciales).
Ejemplo: escribe la formula semidesarrollada del 2 - etil - 3 - metil - 1 - pentanol
Paso 1: Identifica la cadena principal, esta me indica la cantidad de carbonos de la cadena.
Para recordar esto les facilito la tabla de prefijos con la cantidad de carbones que corresponde.

Ejemplo: 2 - etil - 3 - metil - 1 - pentanol
En este ejemplo la cadena principal tiene el prefijo penta (lo que indica que la cadena es de 5 carbonos).
Paso 2: Ubica las ramificaciones y el grupo funcional OH.
Ramificaciones tenemos en el carbono nº 2 -etil y en el carbono nº 3 -metil, el grupo OH está en el carbono nº1
Paso 3: Completa la cadena carbonada los enlaces restantes con hidrógenos, tomando en cuenta la capacidad máxima de enlaces del carbono (4 enlaces) y sabiendo que cada linea en la estructura representa un enlace.
1.3. CLASIFICACIÓN
La clasificación de los alcoholes se hace teniendo en cuenta dos aspectos:
Para escribir la formula semidesarrollada de un alcohol se pueden realizar los mismos pasos o estrategias que se usan para formular alcanos. (Tema que ya fue abordado en clases presenciales).
Ejemplo: escribe la formula semidesarrollada del 2 - etil - 3 - metil - 1 - pentanol
Paso 1: Identifica la cadena principal, esta me indica la cantidad de carbonos de la cadena.
Para recordar esto les facilito la tabla de prefijos con la cantidad de carbones que corresponde.

Ejemplo: 2 - etil - 3 - metil - 1 - pentanol
En este ejemplo la cadena principal tiene el prefijo penta (lo que indica que la cadena es de 5 carbonos).
C -C -C - C -C
Ramificaciones tenemos en el carbono nº 2 -etil y en el carbono nº 3 -metil, el grupo OH está en el carbono nº1
Ejemplo: 2 - etil - 3 - metil - 1 - pentanol
Paso 3: Completa la cadena carbonada los enlaces restantes con hidrógenos, tomando en cuenta la capacidad máxima de enlaces del carbono (4 enlaces) y sabiendo que cada linea en la estructura representa un enlace.
Ejemplo:
1.3. CLASIFICACIÓN
La clasificación de los alcoholes se hace teniendo en cuenta dos aspectos:
- 1.3.1. Clasificación según la posición
del grupo —OH: los
carbonos que portan el grupo OH se clasifican en primarios, secundarios y
terciarios, de acuerdo con el número de carbonos a los que están unidos.
Así, un carbono primario está unido a un carbono, uno secundario, a dos carbonos y uno terciario a tres carbonos. (este tema ya fue abordado de manera presencial).
Tomando en cuenta lo anterior:
Así, un carbono primario está unido a un carbono, uno secundario, a dos carbonos y uno terciario a tres carbonos. (este tema ya fue abordado de manera presencial).
Tomando en cuenta lo anterior:
- Cuando el grupo OH está unido a un carbono primario se considera un alcohol primario.
- Cuando el grupo OH está unido a un carbono secundario se considera un alcohol secundario.
- Cuando el grupo OH está unido a un carbono terciario se considera un alcohol terciario.
- 1.3.2. Clasificación según el número
de grupos —OH presentes: según este parámetro tenemos.
- Alcoholes monovalentes o monoles, dentro de los cuales están todos los ejemplos mencionados anteriormente. Este tipo de alcoholes se caracteriza por tener solamente un grupo -OH.
- Alcoholes divalentes o glicoles, caracterizados por tener dos grupos —OH ejemplo:
- Por último, cuando la molécula posee tres grupos hidroxilo se tiene un alcohol trivalente o glicerol también son llamados polioles:
Es conveniente aclarar que un mismo átomo
de carbono no puede tener dos hidroxilos y si llegara a tenerlos, la sustancia
perdería inmediatamente una molécula de agua, convirtiéndose así en un aldehído
o en una cetona.
1.4. APLICACIONES DE LOS ALCOHOLES MÁS COMUNES
El metanol se conoce comúnmente como alcohol de madera, porque anteriormente se obtenía calentando madera en ausencia de aire. Hoy, este proceso se sigue utilizando, pero sólo para obtener carbón vegetal.
El metanol puro se ha usado durante años, en los motores de los autos de carreras. Su utilización en autos normales no está descartado ya que produce menos monóxido de carbono que la gasolina y además por su resistencia al golpeteo. La inconveniencia de utilizar al metanol como combustible en los autos, es por su tendencia a convertirse en formaldehído, del cual se sospecha puede ser cancerígeno.
El metanol, industrialmente se utiliza en la obtención de formaldehídos, los cuales son usados en la manufactura de polímeros. Se utiliza además como materia prima en la síntesis de ácido acético, ésteres, para desnaturalizar el alcohol etílico, como disolvente y como anticongelante.
El metanol se conoce comúnmente como alcohol de madera, porque anteriormente se obtenía calentando madera en ausencia de aire. Hoy, este proceso se sigue utilizando, pero sólo para obtener carbón vegetal.
El metanol es sumamente venenoso para los seres humanos, su ingestión puede producir ceguera y la muerte, incluso si se ingiere en pequeñas cantidades, puede provocar dolor de cabeza y fatiga.
El etanol se conoce comúnmente como alcohol de caña o alcohol etílico, se encuentra en bebidas como cerveza, vino, whisky, tepache y tejuino. Se produce por fermentación del grano de maíz, sorgo, arroz, cebada, uvas, etc.
El etanol, al igual que el metanol sirve como combustible en motores de combustión interna, y en la actualidad se añade a la gasolina para formar gasohol.
El etanol se utiliza como disolvente en perfumes, saborizantes, barnices, bebidas alcohólicas, medicamentos (como jarabes, tintura de yodo). El etanol se utiliza en la industria y también como antiséptico, se desnaturaliza al adicionarle pequeñas cantidades de metanol, para evitar su consumo como bebida.
El isopropanol, 2-propanol o alcohol isopropílico es un líquido incoloro que hierve a 82.5° C y funde a -89.5° C, se utiliza como materia prima en la elaboración de la acetona, como disolvente de los componentes del shellac y de otros acabados resinosos, como desinfectante y como alcohol de fricción(alcohol para frotar), ya que se evapora con rapidez y enfría la piel, reduciendo el tamaño de los vasos sanguíneos que se encuentran cerca de la superficie y el tamaño de los poros.
El etilenglicol o 1,2-etanodiol es el alcohol más sencillo que contiene dos grupos OH, éste es tóxico cuando se ingiere y provoca daños renales, coma y la muerte.
Una de las principales aplicaciones del etilenglicol en la vida cotidiana, es su uso como anticongelante en los automóviles y como disolvente en la industria de pinturas y plásticos. También se utiliza en las formulaciones de tinta para imprenta y plumas de escribir.
La glicerina o 1,2,3-propanotriol ha encontrado muchas aplicaciones en medicina por su carácter higroscópico, en la preparación de ungüentos, cremas, cosméticos y algunos jabones para el suavizado de la piel y de las manos.
En la industria de la curtiduría encuentra aplicación en la producción de cueros, para proteger a éstos contra el secado: en la industria textíl, para el afino de las telas con el fin de impartirles suavidad, elasticidad, etc. La glicerina se emplea también para la obtención de resinas sintéticas y de sustancias explosivas, por ejemplo, la nitroglicerina.
La fórmula de la glicerina es:

- Ejercicios de autoevaluación de alcoholes
1. Nombra los siguientes alcoholes empleando las reglas de nomenclatura IUPAC.
2. Escribe la fórmula semidesarrollada de los siguientes alcoholes
a) 2 - etil - 3 - metil - 1 - butanol
b) 3 -metil -2-butanol
c) 2 - metil-1-propanol
d) 3,5 - dimetil - 4 - heptanol
3. Hacer clic en este link, para resolver una sopa de letras que se ha creado con términos relacionados al tema.






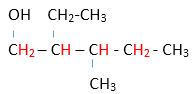





Comentarios
Publicar un comentario